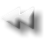Elettroforesi delle Plasmaproteine
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
51
52
53
54
55
Elettroforesi delle plasmaproteine
BIOCHIMICA DELLE PROTEINE
Glicoproteine
· La maggioranza delle plasmaproteine sono glicoconiugati in cui una o più catene di carboidrati o glicani sono legati covalentemente da legami glicosidici a catene laterali di aminoacidi presenti nel polipeptide
· Esistono N-glicani in cui il legame avviene tramite l’atomo di azoto di una asparagina
· Esistono O-glicani in cui il legame avviene di solito con un atomo di ossigeno di una serina o treonina
· La presenza di una ben definita catena di carboidrati è essenziale per le funzioni biologiche della proteina stessa.
Sintesi delle proteine plasmatiche
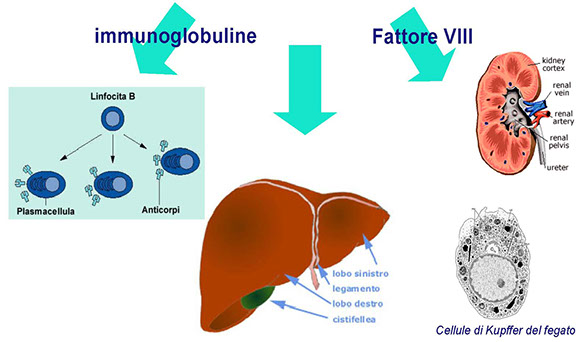
Le proteine plasmatiche sono in equilibrio dinamico con le componenti dei tessuti e dei liquidi biologici
Fattori ormonali (tiroxina e cortisolo aumentano la velocità di sintesi dell’albumina), lo stato nutrizionale e le condizioni generali di salute ne influenzano la sintesi
Presentano un turnover peculiare per ogni frazione e sono degradate ed eliminate, principalmente, a livello epatico e gastrointestinale
BIOCHIMICA CLINICA DELLE PROTEINE
Matrici biologiche
Proteine plasmatiche
Proteine urinarie
Proteine liquorali
Proteine fecali
BIOCHIMICA CLINICA DELLE PROTEINE
Approccio qualitativo e semiquantitativo:
tecniche elettroforetiche
Approccio quantitativo:
tecniche immunochimiche
CRITERI DI RISOLUZIONE
Prealbumina
Eterozigosi della α1antitripsina
Zona α2 sdoppiata: componente anodica = α2-macroglobulina, catodica = aptoglobina
Zona β sdoppiata: β1 = transferrina, β2 = C3
Componenti monoclonali <1g/L e oligoclonalità.
F. Aguzzi, D. Fenili, N. Montalbetti, C. Petrini, F. Salvatore, M. Tarantino
Raccomandazione ufficiale della Commissione SIBioC
L’elettroforesi delle sieroproteine 1° Biochimica Clinica 9; 1985
ELETTROFORESI delle SIEROPROTEINE
Albumina
α1AT
α2macro
APTG
TRF
C3
γ-globuline
(Ig)
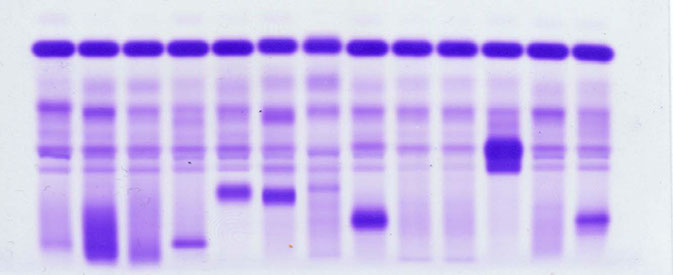
ELETTROFORESI delle SIEROPROTEINE
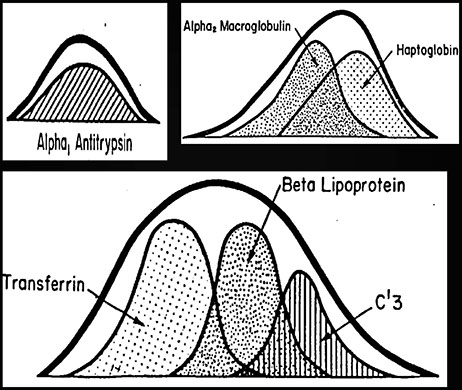
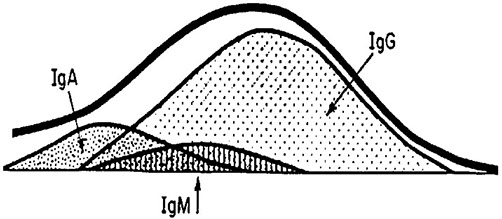
MAGGIORI PROTEINE NELLA BANDA GAMMA
ELETTROFORESI delle SIEROPROTEINE
TRAGUARDI DIAGNOSTICI
· rilevazione e quantificazione delle componenti monoclonali
· rilevazione di varianti genetiche delle proteine
· rilevazione di varianti indotte delle proteine
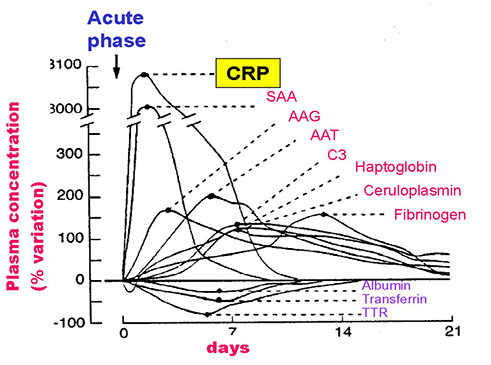
Proteine di fase acuta
GAMMOPATIE MONOCLONALI
Le gammopatie monoclonali rappresentano un gruppo di patologie caratterizzate dalla proliferazione di uno o più cloni plasmacellulari (linfociti B differenziati), ognuno dei quali produce una quantità variabile di immunoglobuline omogenee dal punto di vista strutturale e immunologico che costituisce la componente monoclonale (CM) o paraproteina.
GAMMOPATIE MONOCLONALI
La CM circolante può essere costituita da:
a) un’immunoglobulina completa
b) solo catene leggere
(catene leggere libere, fLC)
c) solo catene pesanti (più raramente)
ELETTROFORESI delle SIEROPROTEINE
APPROPRIATEZZA DELLA RICHIESTA
L’EF delle sieroproteine è l’unica tecnica che consente di evidenziare la presenza di una CM dimostrando l’omogeneità molecolare della Ig.
Sebbene la prevalenza della condizione non giustifichi uno screening di popolazione, sembra ragionevole proporne l’esecuzione all’ammissione in ospedale nei pazienti in età adulta.
Visto che la progressione del rischio è continua, il monitoraggio della concentrazione della CM è un parametro di laboratorio utile e necessario.
Graziani MS, Dolci A et al. Biochim Clin. 2008;32:48-51
ELETTROFORESI delle SIEROPROTEINE
APPROPRIATEZZA DELLA RICHIESTA
L’EF deve essere sempre eseguita quando si sospetta un mieloma, una macroglobulinemia di Waldeström o una MGUS.
L’assenza di CM all’EF non esclude peraltro la presenza di neoplasia dei B linfociti.
In presenza di fondato sospetto clinico è necessario eseguire l’immunofissazione (IFE) del siero e delle urine per la ricerca della BJP.
Risultati e commento
I risultati di questo esame devono esser accompagnati da un “commento “ del laboratorista “validatore”, commento che favorisce la corretta interpretazione dell’analisi ed assicura la sua piena comprensibilità al clinico
Nel caso di riscontro di c.m. oltre al commento è importante associare la quantificazione del picco.
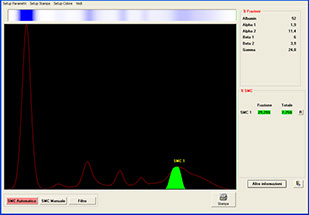
Elettroforesi Proteica a 6 bande
Criteri interpretativi
Quadro elettroforetico delle siero-proteine umane
Identificazione delle frazioni e relative proteine
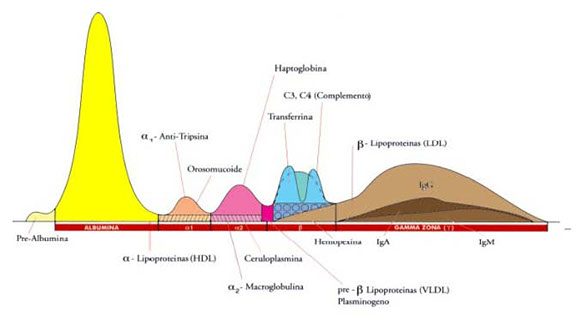
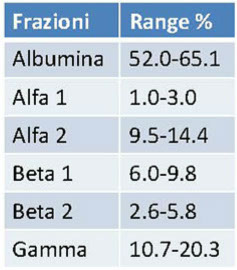
Informazioni da considerare per l’interpretazione
Ciascuna frazione del tracciato elettroforetico deve esser analizzata per la presenza di anomalie qualitative e quantitative
* Frazioni aumentate
* Frazioni diminuite
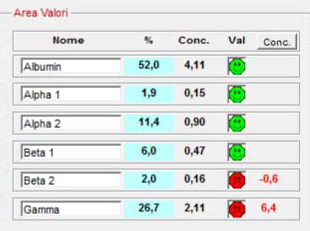
* Presenza di una frazione inusuale aggiuntiva o morfologia inusuale di una frazione (distorsione)
Informazioni da considerare per l’interpretazione
* Aspetto globale del pattern completo
* Colore ed aspetto del siero (emolizzato, itterico, torbido o presenza di precipitato nel siero)
* Concentrazione delle proteine totali
* Considerare l’età del paziente. Qualsiasi paziente al di sopra dei 45 anni è esposto ad un rischio aumentato per la presenza di CM
Altre info da da considerare:
* Presenza di frazioni con flag (< o >) relativo a valori % o in g/L
* Quando possibile: storia del paziente, test precedenti, trattamento terapeutico
* Informazione clinica se disponibile: dolori ossei, perdita di peso, anemia, VES aumentata, ipercalcemia…
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
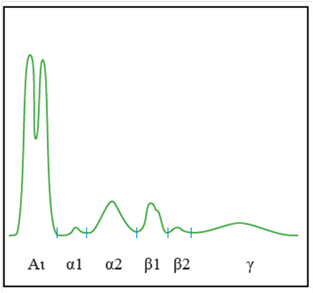


Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Scissione dell’albumina (bis-albuminemia)
· Congenita
Rara anomalia, ereditaria oppure acquisita, caratterizzata dalla presenza, al quadro proteico elettroforetico, di due bande distinte oppure di una singola banda allargata per l’albumina
· Transitoria
Bisalbuminemia indotta da farmaci (soprattutto antibiotici β-lattamici)
Pancreatite (gli enzimi pancreatici possono portare ad uno splitting dell’Albumina)
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Lipoproteine aumentate o pigmenti dovuti a malattie biliari
possono dare una banda distinta tra l’alfa 1 e l’albumina o una spalla sulla frazione albumina (verifica i parametri relativi ai lipidi e il colore del siero).
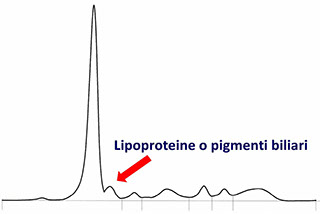
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Aumento delle frazioni α1, α2, β2 con o senza alcun aumento delle immunoglobuline (profilo infiammatorio)
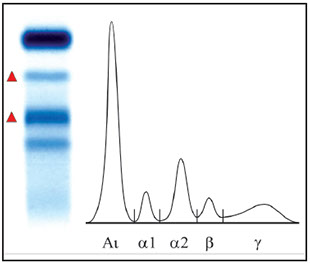
Profilo infiammatorio
Significato clinico
Fattori scatenanti: infezioni, traumi, interventi chirurgici, ustioni, neoplasie e necrosi.
Proteine della fase acuta: hanno funzioni di mediazione (CRP, C3), immunoregolazione (CRP, a1-GA), inibizione (a1-AT, HPT), ricostruzione (a1-GA, a1-AT) e rimozione di prodotti infiammatori (HPT).
Può essere accompagnato da una variazione policlonale o oligoclonale della zona gamma.
Quale è l’accuratezza diagnostica della EP
nell’evidenziare / monitorare una condizione di flogosi?
1. L’EP evidenzia alcune proteine di fase acuta; queste proteine non sono marcatori né precoci né sensibili di flogosi.
2. Essendo una tecnica al più semiquantitativa non è adeguata al monitoraggio della malattia.
L’elettroforesi non è indicata per evidenziare / monitorare situazioni flogistiche
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Aumento isolato della zona alfa 2 con una significante diminuzione della concentrazione delle proteine totali (sindrome nefrotica)
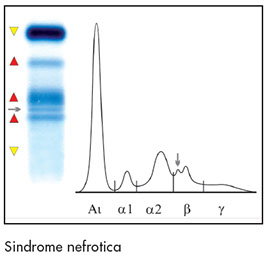
* Sindrome nefrosica
1) Proteinuria:
Generalmente superiore ai 3 g/die
2) Ipoprotidemia:
A causa della perdita urinaria di proteine si verifica:
- riduzione delle proteine totali sieriche (sotto 6 g/dl)
- ipoalbuminemia
- aumento percentuale della a2 e ß2 globuline
- riduzione delle g globuline
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Aumento isolato della fraz. beta 1 (senza deficienza di ferro) associato con una distorsione della fraz alfa 2 (Emolisi: Hb libera in zona beta 1 e complesso Hpt–Hb in zona alfa 2): osservare l’aspetto del siero
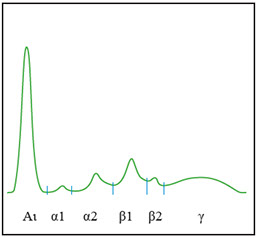

Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Aumento della beta 2 con o senza ipergammaglobulinemia associata e con problema epatico noto o infezione virale (Aumento policlonale delle IgA = Ponte Beta-Gamma)
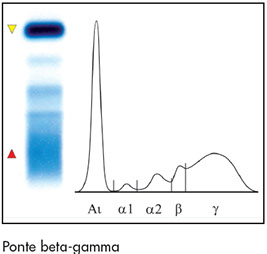
Ponte β-γ
Significato clinico
Il ponte b-g è causato da un marcato aumento policlonale delle IgA che migrano in questa regione, concomitante ad un aumento delle IgM e IgG, che si riscontra nella cirrosi epatica.
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* frazione alfa 1 sdoppiata (differenti fenotipi di A1AT)
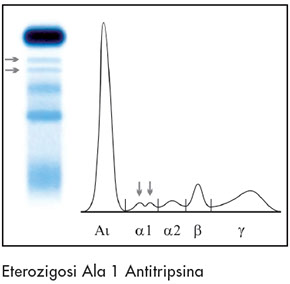
Deficit di A1AT
Significato clinico
L’α1-antitripsina è una glicoproteina responsabile del 90% dell’attività antiproteinasica del plasma.
I fenotipi MZ, SS, SZ e ZZ sono generalmente associati a livelli bassi di α1 antitripsina.
Il fenotipo ZZ si associa nel 20-30% dei casi a cirrosi epatica infantile e nello sviluppo di enfisema polmonare tra 30-40 anni. Questa condizione è causata dalla distruzione del tessuto elastico polmonare da parte di elastasi e collagenasi insufficientemente inibite.
È quindi importante segnalare gli sdoppiamenti e le diminuzioni della zona alfa 1 con la richiesta di un eventuale dosaggio quantitativo per alfa1- antitripsina.
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
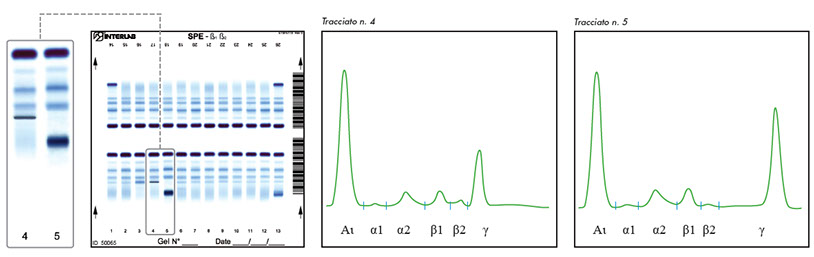
* Distorsione isolata o frazione alfa2 sdoppiata senza aumento del valore di concentrazione della frazione e senza ipogammaglobulinemia (differenti fenotipi di Aptoglobina o leggera emolisi)
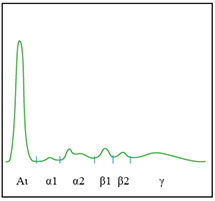
Principali anomalie del pattern elettroforetico che non richiedono un IT o una IF
* Componenti monoclonali precedentemente identificate e caratterizzate (fino a che non avvengono variazioni nell’aspetto del picco o l’insorgere di un nuovo picco sospetto)
CASO CRIOGLOBULINE
Profilo oligoclonale
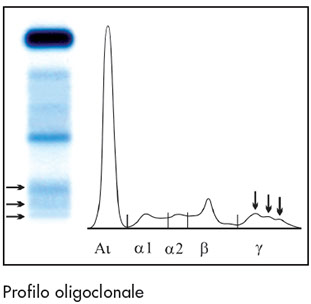
(infezione, virale, malattia autoimmune, trattamento immunosoppressore)
Bande simili a componenti
frequentemente incontrate
Tracciati sierici anormali possono essere dovuti a:
· Condizioni patologiche
· Condizioni fisiologiche
· Impropria conservazione del campione
· Fenotipi o varianti di proteine normalmente presenti
· Sostanze esogene
Proteine fisiologiche che assomigliano a componenti monoclonali
La degradazione del complemento (C4) dà un picco
addizionale in zona Beta 2 (spalla a sx della frazione Beta 2)
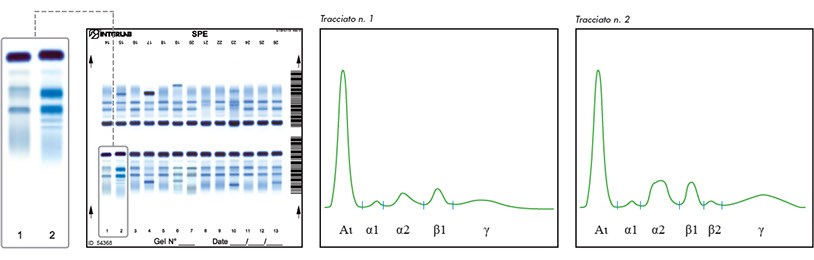
Proteine fisiologiche che assomigliano a componenti monoclonali
Proteine della fase acuta: la PCR al di sopra di 250 mg/L (variabile secondo il fondo policlonale ) può risultare in una debole frazione addizionale in zona gamma (verso la zona beta2). Di solito la PCR aumentata è associata con un profilo infiammatorio (aumento di alpha 1, alpha 2 e beta 2).
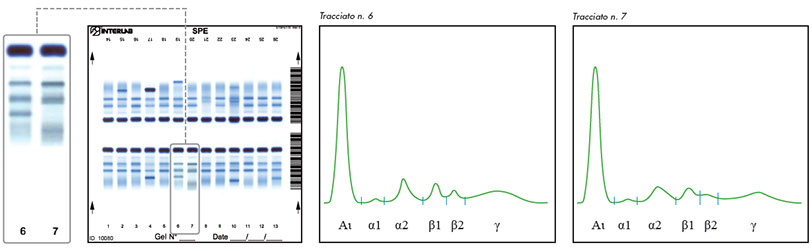
Proteine fisiologiche che assomigliano a componenti monoclonali
La presenza di Fibrinogeno nel plasma o campioni non completamente coagulati, presentano una banda addizionale molto vicina (o all’interno) della frazione beta 2.
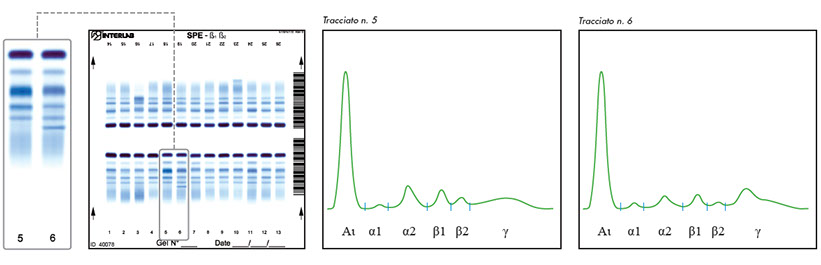
Proteine fisiologiche che assomigliano a componenti monoclonali
Fibrinogeno: rimozione dell’interferenza
Il trattamento del campione di siero con trombina, reptilasi o etanolo consente di rimuovere l’interferenza da fibrinogeno
Agarosio: trattare 90 ul di siero con 10 ul di etanolo puro; lasciare tutta la notte a 4°C, centrifugare ed eseguire l’elettroforesi.
Capillare: 270 ul di siero + 30 ul di etanolo
DEFINIZIONE DI CM COME ANALITA
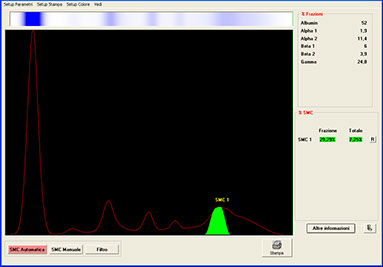
Ogni CM è costituita da una frazione elettroforetica omogenea dal tipico aspetto morfologico di picco alto e stretto.
Perché è importante refertare anche
le piccole componenti monoclonali nel siero?

È importante refertare ogni C.M.
Perché è importante refertare anche
le piccole componenti monoclonali nel siero?

E’ importante refertare la C.M.
nel contesto del tracciato elettroforetico.
ELETTROFORESI delle SIEROPROTEINE
QUANTIFICAZIONE DELLA CM
· porre diagnosi differenziale tra MGUS (CM <30 g/L) e MM (CM >30 g/L)
· valutare il rischio di progressione di una MGUS verso il mieloma, che è continua e non si stabilizza nel tempo
· valutare in corso di mieloma e disordini correlati, la risposta alla terapia
ELETTROFORESI delle SIEROPROTEINE
QUANTIFICAZIONE DELLA CM

Leukemia 2006;20:1467-73
COME SI MISURANO LE CM
Ogni CM rilevata alla EF va quantificata sul tracciato mediante lettura:
· densitometrica in AGE o
· spettrofotometrica in CZE.
COME SI MISURANO LE CM
La quantità di CM deriva dalla misura percentuale dell’area del picco, a partire dalla linea di base, e dal calcolo ricavato sulla base della concentrazione delle proteine totali del campione.
COME (NON) SI MISURANO LE CM
The fundamental disadvantage of the immunochemical technique is its inability to distinguish between monoclonal and polyclonal Igs. This is particularly important in follow-up because worsening of the disease is associated with an increase of MC and a decrease of polyclonal Igs.
Merlini G. JIFCC 1997;9:171-6
COME (NON) SI MISURANO LE CM
La quantificazione della immunoglobina monoclonale con metodi immunochimici è inaccurata perché il calibratore (policlonale) ed il campione (monoclonale) non reagiscono allo stesso modo con l’antisiero contenuto nel saggio (mancanza di parallelismo) e perché la proteina monoclonale può presentare specificità antigeniche poco o mal riconosciute dall’antisiero stesso.
Graziani MS. Biochim Clin. 2008;32:48-51
SPE: valutazione qualitativa & quantitativa
· Paziente in follow-up con CM caratterizzata con IF
· Ipogamma w/o picco visibile
· CM nota & nessun picco visibile
· BJ nelle urine e assenza di CM nel siero
· Leggero aumento isolato di α2, β1 o β2 (senza alcun anomalia sul pattern proteico)
· Pattern normale
· Infiammatorio
· Nefrotico
· Doppia α1 or α2
· Bisalbuminemia
· Emolisi
· Iperlipemia
· Ponte β-gamma
· CM nota
Fare IF
Stop Investigation
Evidenza di anormalità
Pattern
discutibile
Evidenza di
anormalità
Nessun anormalità
rilevata
Pattern
discutibile
Assenza di gammopatia
Ripetere
fra 3 mesi
Gammopatia
>