Significato clinico delle Proteine Plasmatiche
Significato clinico delle Proteine Plasmatiche
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
51
52
53
54
55
56
57
58
59
60
61
62
63
64
65
66
67
68
69
Significato clinico delle proteine plasmatiche

Prealbumina
α2-macroglobulina
Fraz.C3
complemento
γ-globuline
PROTEINE DEL PLASMA
Le proteine del plasma costituiscono un gruppo eterogeneo di proteine, ognuna delle quali possiede una funzione specifica o raggruppa in se diverse funzioni ed è soggetta a specifiche variazioni di concentrazione in svariate condizioni fisiologiche e patologiche.
La sintesi di ciascuna proteina è sotto stretto e specifico controllo genico e la sua normale concentrazione plasmatica varia da pochi microgrammi ad alcuni grammi per litro.
La misure delle concentrazioni delle proteine plasmatiche è quindi di valido aiuto nella diagnosi e nella gestione di diverse condizioni fisiopatologiche.
PROTEINE DEL PLASMA
· I metodi di separazione e di misurazione impiegati rispecchiano in prevalenza aspetti molecolari, chimici, fisici o la loro funzione, un’identica sostanza viene molte volte, a seconda delle circostanze e del metodo impiegato, denominata in diversi modi: macroglobulina, immunoglobulina M, γ-globulina, glicoproteina.
· È quindi importante lo studio delle caratteristiche strutturali, metaboliche e funzionali delle numerose proteine del plasma e delle loro variazione genetiche.
· Altrettanto importante è il valore clinico da attribuire alle modificazioni dei singoli elementi o alle variazioni multiple nella diagnosi e nel monitoraggio delle malattie.


CARATTERIZZAZIONE DELLE PROTEINE DEL PLASMA
A) Caratteristiche chimiche: proteine semplici, glicoproteine, lipoproteine
B) Caratteristiche chimico-fisiche: solubilità, sedimentazione, migrazione elettroforetica
C) Caratteristiche funzionali: enzimi, proteine di trasporto, della coagulazione, della cascata del complemento, di controllo della crescita e del differenziamento, delle difese immunitarie, d’integrazione del metabolismo.
PRECIPITAZIONE FRAZIONATA MEDIANTE SOLVENTI ORGANICI
Vengono utilizzati solventi organici miscibili con acqua
Alcooli
Acetone
Diossano
}
I solventi mischiati con l’acqua determinano
DISIDRATAZIONE DELLE MOLECOLE PROTEICHE
AGGREGAZIONE DELLE PROTEINE

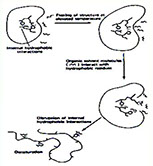
Per prevenire la denaturazione delle proteine, il frazionamento deve essere compiuto a bassa temperatura (0°C) ed in ambiente in grado di assorbire velocemente il calore sviluppatosi in seguito al mescolamento del solvente organico con l’acqua (bagno di ghiaccio).
SEDIMENTAZIONE
Mediante ultracentrifugazione è possibile conoscere la massa molecolare delle particelle che sedimentano
Svedberg: il coefficiente di sedimentazione è definito come la velocità di sedimentazione in un campo di forza unitaria (velocità/forza centrifuga)
Il coefficiente di sedimentazione di una molecola dipende dalla:
}
MASSA MOLECOLARE
FORMA (ellissoide, sfera, bastoncino) e DENSITÀ (sfera compatta, pallone vuoto)
DIMENSIONI
DENSITÀ E VISCOSITÀ DEL MEZZO CIRCOSTANTE
Coefficiente di frizione
di una molecola sferica può essere calcolata con l’equazione di Stokes
La legge non soddisfa più quando la forma si allontana da quella di una sfera compatta e a temperature > 20°C
RIASSUMENDO: la velocità di sedimentazione di una particella è proporzionale alla sua massa, ma una molecola più densa sedimenta più velocemente di una meno densa a parità di densità della soluzione. Inoltre, il coefficiente di frizione aumenta moltissimo procedendo dalla forma ellissoide a quella a sigaro o a bastoncino.
MIGRAZIONE ELETTROFORETICA
Il termine elettroforesi fu applicato in origine al movimento, sotto l’influenza di un campo elettrico, di ioni o di molecole di diversa grandezza, provviste di carica netta e disciolte in soluzione.
Le proteine in soluzione sono facilmente ionizzabili e si dissociano in ioni R-COO- oppure ioni R-NH3+.
Analiti
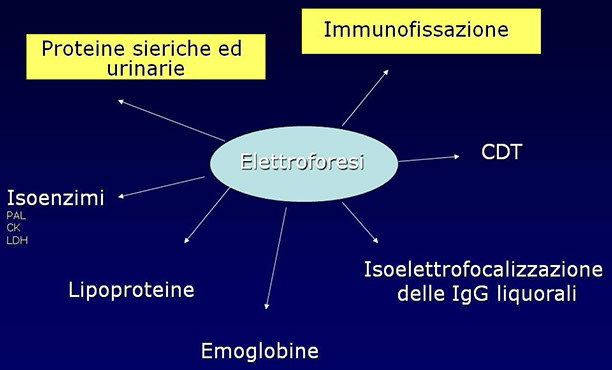
Elettroforesi zonale
Nel profilo elettroforetico ottenuto sono distinguibili delle zone in cui migrano una o più proteine specifiche
IN FASE SOLIDA
AGAROSIO,
(Acetato di cellulosa)
IN FASE LIQUIDA
CAPILLARE RIEMPITO
DI UN TAMPONE
Parametri che influenzano la migrazione elettroforetica


SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
1. Il tracciato elettroforetico è rimasto uno dei pochi esami di laboratorio in cui l'interpretazione del risultato non si basa su un valore numerico confrontabile con un intervallo di riferimento definito in soggetti “normali”.
2. L’ interpretazione visiva di un tracciato risente di variabili dovute alla tecnica ed alla strumentazione, ma anche all'operatore.
3. Per questo motivo è indispensabile una stretta collaborazione ed un attivo interscambio tra chi esegue l'esame e chi lo interpreta.
PROTEINE PLASMATICHE
Per l’analisi sono raccomandati campioni freschi.
I sieri devono essere prelevati seguendo le procedure convenzionali per i test clinici di laboratorio.
I sieri vanno refrigerati (2-8 °C) e si possono conservare fino ad una settimana.
Se necessitano periodi di conservazione più lunghi mantenere i campioni congelati a -20°C (fino ad un mese)
CAMPIONI DA EVITARE
· Non utilizzare campioni di siero emolizzati
· L'emolisi causa un aumento delle zone alfa-2 e beta.
· Evitare campioni di plasma
· Evitare campioni vecchi o mal conservati o francamente lipemici
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
· Fornisce informazioni su ALCUNE proteine rispetto alle oltre 100 che si trovano nel siero, perché quantitativamente più rappresentative nelle singole bande.
· Tuttavia tali informazioni hanno in taluni casi (es. componenti monoclonali, deficit di alfa 1-antitripsina, sindrome nefrosica ecc.) un significato clinico importante ed immediato.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
1. Le proteine plasmatiche costituiscono un pool in equilibrio dinamico modulato dalla velocità di sintesi e di catabolismo delle singole entità proteiche.
2. Qualsiasi evento capace di modificare una delle due velocità provoca una variazione del tasso ematico della proteina.
3. Le proteine plasmatiche sono sintetizzate in netta prevalenza dal fegato ad eccezione delle immunoglobuline sintetizzate dalle plasmacellule,di alcuni componenti del complemento sintetizzati almeno in parte dai macrofagi e di alcune lipoproteine dalle cellule intestinali.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
Le proteine totali nel sangue si possono dosare sia su plasma che su siero.
Per problemi di strumentazione automatica il dosaggio si effettua quasi esclusivamente su campioni di siero.
Gli intervalli di riferimento normali per le proteine del siero sono tra 60 e 84g/L.
Per il plasma, la proteinemia totale è più alta del 3-5% per la presenza del fibrinogeno.
I valori sierici non sono costanti in tutta la vita: alla nascita le proteine del siero ammontano a 55,2 g/L ed il rapporto albumina/globuline e alto (2,10).
Le concentrazioni sieriche nell’infanzia son più basse rispetto all’età adulta e nelle donne sono leggermente inferiori rispetto a quelle dell’uomo.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
Oltre all’età e al sesso, altri fattori possono far variare la protidemia:
1. variazioni cospicue in ambito fisiologico possono esserci nell’arco della giornata
2. variazioni stagionali con picchi a novembre e diminuzioni massime a giugno,
3. aumenti dopo esercizio fisico,
4. diminuzioni in soggetti bloccati a letto.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
· I livelli plasmatici fisiologici dipendono dalla sintesi, dal catabolismo, dalla diminuzione delle proteine nei vari compartimenti corporei e da perdite esterne.
· Questi fattori devono essere tenuti in considerazione anche durante lo sviluppo di una patologia,poiché le modifiche contemporanee di alcune condizioni (ad esempio aumentata sintesi ed aumentato catabolismo) possono risultare in un livello normale della componente proteica.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
· Le plasmaproteine vengono sintetizzate principalmente dal fegato, in particolare l’albumina, il fibrinogeno e le globuline, ad eccezione delle immunoglobuline che vengono prodotte dal sistema immunitario (plasmacellule).
· Contribuiscono alla sintesi anche l’intestino per le lipoproteine ed il sistema monocito/macrofagico per alcuni fattori del complemento.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
· Il metabolismo delle proteine è rapido ed intenso: viene giornalmente rinnovato, in condizioni fisiologiche, il 9% di tutte le proteine sintetizzate dal fegato ed il 10-25% di quelle circolanti.
· Anche nel catabolismo gioca un ruolo fondamentale il fegato.
· In condizioni fisiologiche le perdite (esterne) avvengono attraverso l’apparato gastroenterico (tutte le proteine), il rene (selettivo), le ghiandole esocrine, l’apparato respiratorio e gli organi genitali.
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
· Funzionalmente possono essere divise in:
1) Immunoglobuline con funzione anticorpale
2) Proteine di trasporto
3) Fattori del complemento
4) Inibitori delle proteasi
5) Varie: proteine della fase acuta, fattori della coagulazione, lipoproteine, glicoproteine, etc.
CRITERI DI RISOLUZIONE DELL’EF

F. Aguzzi, D. Fenili, N. Montalbetti, C. Petrini, F. Salvatore, M. Tarantino
Raccomandazione ufficiale della Commissione SIBioC
L’elettroforesi delle sieroproteine 1° Biochimica Clinica 9; 1985
RIVELAZIONE EF IN FASE SOLIDA
Acetato
di cellulosa
+
Rosso Ponceau
= 0.14 g/L
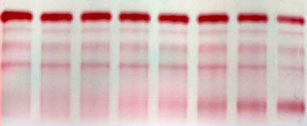
Agarosio
+
Acid Blue
= 0.04 g/l
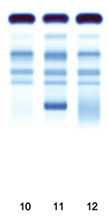
Utilizzo di gel d’agarosio o acetato di cellulosa DIAFANIZZAZIONE
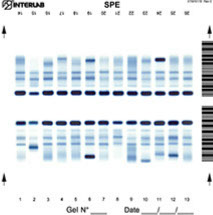
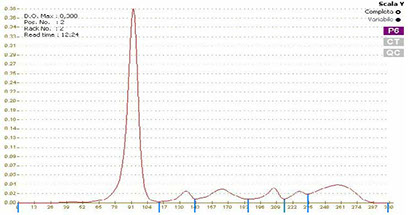
I tracciati vengono letti mediante SCANSIONE FOTODENSITOMETRICA: trasforma le differenze di intensità in un grafico con picchi di base e altezza variabili secondo l’ampiezza e l’intensità della zona separata e colorata (quantificazione qualitativa-semiquantitativa)
In un siero normale i valori espressi in percentuale delle frazioni proteiche (elettroforesi a 5 zone) sono:
albumina 55-65%
α1 2-5%
α2 7-11%
β 9-13%
γ 14-20%
Evidenzia solo variazioni qualitative delle proteine del siero.
Intensità del picco non corrisponde alla quantità delle proteine perché ogni colorante possiede affinità diversa per le diverse proteine
La proteina che principalmente contribuisce ad una data frazione non è la sola che migra in quella zona, ad eccezione dell’albumina, che può essere considerata unica.
Si preferisce l’ispezione visiva (qualitativa) delle strisce
Elettroforesi Zonale (EF)
L’EF è una tecnica separativa in grado di evidenziare le proteine che si distribuiscono in un campo elettrico in base al al loro punto isoelettrico, ma non fornisce indicazioni sicure e dirette sulle PT che compongono una zona.
L’EF è costituita da tre fasi:
· Separazione in genere in tampone a pH alcalino.
· Rivelazione con un colorante delle PT la cui sensibilità varia a seconda del colorante usato.
Rosso Ponceau-Amido black 1000mg/L
Coomassie brilliant blue 75-300mg/L
Cristal Violet 30mg/L
Oro Colloidale 1-6mg/L
Oro +silver enhancement 0,8-1mg/L
· Lettura e interpretazione
SIGNIFICATO CLINICO DELLE PROTEINE PLASMATICHE
· La valutazione delle bande elettroforetiche rappresenta un valido supporto diagnostico:
· Offre una panoramica su proteine che intervengono in tutti i processi funzionali più importanti delle sieroproteine.
· Permette di rivelare variazioni nella concentrazione di singole proteine o gruppi di proteine, l'eterogeneità di talune frazioni (varianti genetiche), la presenza di paraproteine.
Indicazioni del test

Referto generico di “tracciato elettroforetico nella norma”

Ricevuti i dati, si procede alla loro refertazione
Referto con indicazione qualitativa e quantitativa (aumento o diminuzione) delle frazioni proteiche alterate
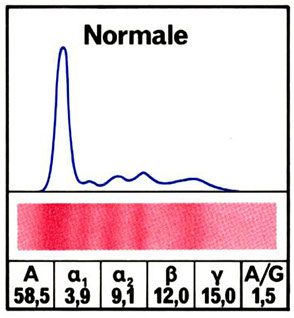
PROTEINE SIERICHE
Concentrazione normale: 65-80 g/l
Fegato
Origine:
Tessuto linfoide
Iperprotidemie: aumento proteine specifiche (disglobulinemie) emoconcentrazione
Ipoprotidemie: diminuzione delle proteine (difetti di assorbimento, apporto, perdita proteica, insufficienza epatica) emodiluizione

L’elettroforesi delle proteine sieriche
su gel di agarosio e su capillare
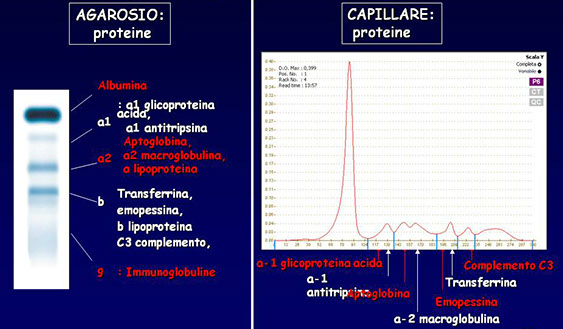
BANDA PREALBUMINICA
· La PREALBUMINA è la banda più anodica che si presenta all'elettroforesi.
· È visibile nel tracciato non diafanizzato e questa semplice osservazione è sufficiente a rilevarne la diminuzione.
· È una proteina di trasporto il cui significato diagnostico è quello di indicatore assai sensibile dello stato nutrizionale dell'organismo, insieme ad albumina e transferrina;
· la sua emivita molto breve (1,9 giorni) permette di valutare velocemente le variazioni protodosintetica del fegato.
Prealbumina
BANDA ALBUMINICA
ˑ L'ALBUMINA è la principale proteina del siero (60% massa proteica plasmatica), presente in concentrazioni di 40-50 g/litro.
ˑ Ha due funzioni principali: di trasporto (acidi grassi, bilirubina, ormoni, farmaci) e di regolazione della pressione colloidosmotica a cui contribuisce per l'80%;
ˑ una sua diminuzione marcata è indice di uno squilibrio tra la pressione idrostatica e quella oncotica, il plasma esce dai vasi ed impregna i tessuti instaurando l'edema.
ˑ Esistono varianti genetiche dell'albumina a trasmissione ereditaria - alloalbumine o bisalbumine - che si presentano all'elettroforesi con uno sdoppiamento della frazione in cui la variante può essere più lenta o più veloce dell'albumina normale. Queste varianti non rivestono significato clinico e il loro riscontro è quasi sempre occasionale.

BANDA ALBUMINICA
ˑ Sdoppiamento: bisalbuminemie genetiche o transitorie.
ˑ Diminuzione: per deficit di sintesi (epatopatie); per aumentata perdita (sindrome nefrosica, enteropatie proteino-disperdenti, ustioni); diminuzione modesta nella fase infiammatoria acuta ed in gravidanza.
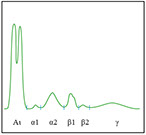
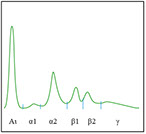
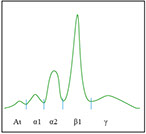
BANDA ALFA 1
ˑ Rispecchia praticamente il livello sierico di ALFA1-ANTITRIPSINA (AAT) che fisiologicamente è il più importante inibitore delle proteasi dei granulociti neutrofili.
Questa funzione ha l'effetto di limitare i processi infiammatori con massiccio intervento di neutrofili, bloccando l'azione distruttiva degli enzimi proteolitici liberati dai loro granuli o con la morte in situ dei neutrofili stessi.
ˑ La regolazione genetica della sintesi e secrezione di questa proteina è molto complessa, presieduta da un grande numero di alleli; il risultato fenotipico è che, nell'ambito di una popolazione, si possono trovare numerose varianti della proteina, per la maggior parte senza conseguenze sulla sua funzione.
BANDA ALFA 1
ˑ Talora la presenza di una AAT variante si esprime con uno sdoppiamento della banda alfa 1 dei quadro elettroforetico: tale reperto va segnalato.
ˑ L'espressione di alcuni alleli si traduce in una sintesi deficitaria (allele Null) o in una mancata liberazione in circolo della proteina (allele Z), con risvolti clinici importanti.
BANDA ALFA 1
· In caso di un suo deficit grave non vengono neutralizzate le proteasi liberate dai granulociti e dai macrofagi, richiamati a livello broncoalveolare in corso di processi microinfiammatori,inducendo all'alterazione distruttiva delle pareti connettivo-elastiche degli alveoli configurando così la condizione clinica nota come enfisema polmonare.
· In alcuni casi poi la proteina viene sintetizzata ma non secreta in circolo dagli epatociti per cui si ha un notevole accumulo intracellulare che configura un grave danno epatico con evoluzione in cirrosi, già durante l'infanzia.
BANDA ALFA 1
ˑ L'alfa 1 antitripsina aumenta tipicamente nelle condizioni infiammatorie dei tessuti di derivazione epiteliale e per tale motivo rientrava in passato nel gruppo delle "proteine della fase acuta".
ˑ Va ricordato che in alcuni (non frequenti) casi, la presenza di due bande alfa 1 è dovuta ad alti livelli di ALFA1-FETOPROTEINA, marcatore, dopo il secondo anno di età, di tumori disembriogenetici, di carcinoma epatico primitivo, di epatiti evolutive, eventualità che vanno comunque conosciute e tenute presenti.
BANDA ALFA 1
· Diminuzione: deficit genetico di alfa1-antitripsina omo- od eterozigote.
· La segnalazione va accompagnata dal dosaggio immunologico quantitativo.
· Aumento. infiammazione acuta
· Sdoppiamento: alfa1-antitripsina variante (non patologico). Presenza di alfa-fetoproteina?
BANDA ALFA 2
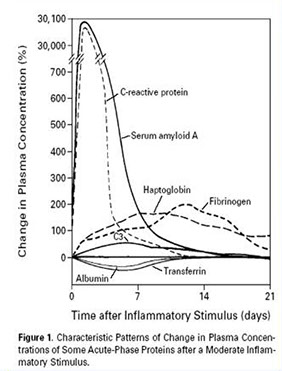
· In questa banda sono risolvibili due componenti: una anodica ed una catodica. La componente anodica è riferibile alla ALFA2-MACROGLOBULINA.
· L' Alfa2-Macroglobulina è una delle proteine plasmatiche a più elevato peso molecolare è un potente inibitore delle proteasi ed interviene sia c nei meccanismi di difesa contro le proteasi endogene, che nell'omeostasi e nell'equilibrio dei processi coagulativi e fibrinolitici.
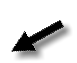
A2-Macroglobulina

BANDA ALFA 2
ˑ Il funzionamento di questa proteina si esplica mediante l'assunzione di proteasi da altri inibitori, seguita dalla loro eliminazione dal circolo.
ˑ Inoltre veicola ormoni come l'insulina ed il somatotropo: in rapporto a quest'ultima funzione, durante l'infanzia è presente in concentrazioni molto più elevate che nell'adulto.
ˑ Anche se è una proteina di grande attività funzionale ha a tutt'oggi un significato clinico abbastanza scarso.
BANDA ALFA 2
ˑ Diminuzione: enteropatie disperdenti eclampsia, artrite reumatoide.
ˑ Aumenti fisiologici: infanzia, gravidanza.
ˑ Aumenti patologici: sindrome nefrosica, fase acuta.
BANDA ALFA 2
· La zona più catodica della banda alfa2 è costituita dall'APTOGLOBINA. Con questo termine si indica in realtà una famiglia di glicoproteine plasmatiche. La loro struttura è determinata geneticamente da due alleli autosomici codominanti Hp 1 e Hp 2 che si esprimono in tre fenotipi: Hp 1 - 1, Hp 1-2 e Hp 2-2.
· Tali proteine hanno P.M. diverso e quindi diversa velocità di migrazione elettroforetica: è per questo che la componente aptoglobinica della banda alfa2 può variare leggermente di posizione

BANDA ALFA 2
La principale funzione dell'aptoglobina è quella di legare l'emoglobina libera nel plasma.
In condizioni fisiologiche una piccola quota di globuli rossi viene distrutta all'interno della circolazione (emolisi intravascolare) con conseguente emoglobinemia.
Questa emoglobina libera viene legata dall'aptoglobina con un rapporto molare di 1: 1.
Il complesso aptpglobina-emoglobina non passa il filtro renale e tende ad essere captato molto rapidamente dal sistema istiocitario macrofagico ed eliminato.
BANDA ALFA 2
· Diminuzioni:
- per iperconsumo: condizioni emolitiche
(anemie emolitiche, eritropoiesi inefficace, accidenti trasfusionali, emolisi da protesi valvolari, anemie megaloblastiche, mononucleosi infettiva, ematomi, emorragia intratissutale, esercizio fisico prolungato).
- per difetto di sintesi: riduzione del parenchima epatico funzionante (epatiti, cirrosi, tumori).
La diminuzione va refertata accompagnata dal dosaggio quantitativo.
· Aumenti:
- processi infiammatori
- processi necrotici
- processi neoplastici
Altre proteine presenti in concentrazioni minori in zona Alfa-2 sono:
CERULOPLASMINA: glicoproteina. Maggiore proteina di trasporto plasmatico del rame.
La sua sintesi avviene nel fegato, ma la regolazione della sintesi è indipendente dalla quantità di rame in circolo.
Ogni molecola si lega a 6 atomi di rame.
Trasporta il rame, normalmente conservato nel fegato, ai tessuti periferici, dove viene utilizzato per la sintesi di numerosi enzimi.
Diminuzione dei livelli di ceruloplasmina si osservano nel morbo di Wilson, caratterizzato da elevati depositi tossici di rame nel fegato, cervello, cuore.
PROTEINA TRASPORTATRICE DELLA VITAMINA D: non si conosce bene la sua funzione specifica, ma è la maggior proteina trasportatrice della vitamina D e dei suoi metaboliti. Sintetizzata del fegato.
BANDA BETA 1
· È costituita fondamentalmente dalla TRANSFERRINA. È stata descritta in letteratura una malattia caratterizzata da assenza congenita di transferrina e quindi da assenza di banda beta 1.
· Esistono transferrine strutturalmente diverse, tutte a migrazione beta1; ogni individuo possiede transferrina di un solo tipo, assai raramente di due tipi.
· Anche se infrequente, questa eterozigosi, che si traduce ne!lo sdoppiamento della banda beta 1 in due componenti sottili, può falsare la ricerca di una componente monoclonale.
BANDA BETA 1
· Lo sdoppiamento può anche essere dovuto alla presenza di un tipo di transferrina caratterizzata da uno scarso contenuto di residui sialici; questa situazione può verificarsi in pazienti epatopatici gravi ed alcoolisti.
· È nota l'importanza funzionale di questa proteina nel metabolismo del ferro.
· Le diminuzioni della transferrina sono di scarso significato diagnostico e sono riferibili a diminuita sintesi epatica.
· Con prealbumina ed albumina, è un indice dello stato nutrizionale di un soggetto.
BANDA BETA 1
ˑ Diminuzioni: per difetto di sintesi :
ˑ epatopatie infezioni croniche ed acute neoplasie anemie da malattia cronica
ˑ per perdita renale: nefrosi glomerulonefrite
ˑ Aumenti fisiologici: gravidanza.
ˑ Aumenti patologici: anemie da carenza di ferro.
BANDA BETA 2
· È costituita principalmente dalla frazione C3 del complemento.
· È visibile soprattutto nel SIERO FRESCO, in quanto il C3 si converte, con l'invecchiamento del siero (anche mantenuto a +4°) nei suoi prodotti di clivaggio che hanno mobilità beta 1.
· Il C3 è la più importante proteina del complemento su cui convergono la via classica e la via alternativa di attivazione.
BANDA BETA 2
· È l'unico componente della cascata complementare visualizzabile sul tracciato elettroforetico, quindi attraverso l'analisi ispettiva della banda beta2 possiamo trarre significative informazioni sullo stato di attività funzionale di questo sistema di proteine così importante per i meccanismi di difesa dell'organismo.
BANDA BETA 2
ˑ Il riscontro di una banda beta2 di diminuita intensità o addirittura assente è associato a una riduzione del C3.
ˑ Questo dato va sempre confermato con il dosaggio nefelometrico della proteina e poi segnalato nel referto.
BANDA BETA 2
· Diminuzioni:
- forme acquisite: per iperconsumo:
glomerulonefriti LES batteriemie artriti
per diminuita sintesi: epatopatie
-forma congenita (molto rara)
siero "vecchio“
· Aumenti:
- processi infiammatori non recenti
- processi infettivi
- processi tumorali
- infarto del miocardio
- ostruzioni biliari
PROTEINA C REATTIVA
· È una proteina che si riscontra nel siero di soggetti affetti da disordini di tipo infiammatorio; come la VES, è estremamente aspecifica ma se presente in concentrazioni sufficientemente elevate, può comparire all'elettroforesi come una banda ristretta in zona gamma catodica simulando una componente monoclonale.
ZONA GAMMA
· Tale zona è costituita essenzialmente dalle IMMUNOGLOBULINE (anticorpi) che costituiscono un gruppo molto eterogeneo di proteine migranti dalla regione beta alla regione gamma e, in taluni casi molto più anodicamente fino alla zona alfa.
· La funzione principale delle immunoglobuline, sintetizzate dalle plasmacellule, è quella di riconoscere antigeni estranei all'organismo e di promuoverne l'eliminazione o comunque favorirne la neutralizzazione (immunità umorale).
· Gli antigeni in causa possono essere noti (come nelle malattie infettive), sospetti o in discussione (come nelle malattie autoimmuni), o difficili da definire (come nelle epatopatie croniche o nella sarcoidosi).
ZONA GAMMA
ˑ È indispensabile una buona risoluzione all’elettroforesi della zona gamma in quanto l'ispezione visiva è determinante nel riconoscere anche piccole alterazioni qualitative importantissime ai fini diagnostici che possono sfuggire alla lettura densitometrica.
ˑ Le 5 classi immunoglobuliniche (G,A,M,D,E) sono presenti in concentrazioni molto variabili nei liquidi biologici in base alle loro funzioni e caratteristiche strutturali; nel siero, la concentrazione dipende dal rapporto sintesi/catabolismo, rapporto che varia per ogni classe e sottoclasse in funzione dell'età, dei sesso, dell'intensità' della stimolazione antigenica oltre che da cause esogene come l'azione dei farmaci.
ZONA GAMMA
· Lo studio delle immunoglobuline permette di riconoscere varie alterazioni schematizzabili nei seguenti tipi:
1) alterazioni quantitative in difetto.
2) alterazioni quantitative in eccesso.
3) alterazioni qualitative.
ZONA GAMMA
· Le sindromi da immunodeficienza, sia congenita che acquisita, sono caratterizzate da un'alta suscettibilità alle infezioni e, talvolta, a malattie autoimmuni e neoplasie linforeticolari.
· Fisiologicamente l'ipogammaglobulinemia è un reperto caratteristico dell'infanzia che talora può anche prolungarsi nel tempo ma è sempre reversibile (ipogammaglobulinemia transitoria dell'infanzia).
ZONA GAMMA
· I deficit primitivi con localizzazione cromosomica dei difetto hanno un'incidenza variabile (es.: agammaglobulinemia legata al sesso: 1150000, deficit selettivo di IgA: 11600).
· L'ipogammaglobulinemia è facilmente identificabile all'elettroforesi quando riguarda le 3 classi immunoglobuliniche principali o almeno le IgG.
· Il deficit selettivo di IgA, si associa ad infezioni del tratto respiratorio, gastroenterico e urogenitale, dove normalmente le IgA sono gli anticorpi più rappresentati, non è individuabile in quanto mascherato dalle altre classi immunoglobuliniche il cui livello è normale o addirittura aumentato per compensazione.
ZONA GAMMA
· Le ipogammaglobulinemie secondarie, cioè non legate a difetti congeniti del sistema immunocompetente sono molto frequenti:
· per riduzione della sintesi o aumento del catabolismo (malnutrizione, malattie linfoproliferative, farmaci immunosoppressori, terapie radianti, gammapatie monoclonali);
· per aumentate perdite (sindrome nefrosica, enteropatieproteino-disperdenti, ustioni).
· Il rilievo all'elettroforesi di ipogammaglobulinemia in adulti o anziani deve sempre attirare l'attenzione sulla probabile esistenza di malattie immunoproliferative (linfomi, mieloma micromolecolare).
ZONA GAMMA
· La produzione in eccesso di immunoglobuline con interessamento di un gran numero di stipiti cellulari immunocompetenti è la fisiologica risposta umorale dell'organismo al contatto con agenti patogeni esterni.
· Prima di essere evidente sul tracciato EP l’ipergammaglobulinemia, nelle infezioni acute richiede un considerevole periodo di tempo - circa 20 giorni - dall'avvenuto contatto antigenico.
· In patologie croniche associate ad aumenti policlonali (epatopatie croniche, malattie del collagene) spesso l'antigene responsabile della reazione anticorpale è un autoantigene verso cui il sistema immune ha perso la tolleranza.
ZONA GAMMA
· Aumentano quasi sempre le IgG, eccezione delle malattie epatiche dove vi è prevalente aumento delle IgA e delle malattie infettive parassitarie dove aumentano le IgM.
· Nelle cirrosi biliari dove il tracciato si caratterizza per l'aumento del "fondo"della zona gammaglobulinica le immunoglobuline coinvolte sono diverse per classi e sottoclassi e quindi presentano un ampio spettro di mobilità elettroforefica.
ZONA GAMMA
· Un particolare profilo della zona gamma può indirizzare il laboratorista verso la classe immunoglobulinica :
nel caso delle IgG un aumento diffuso su tutta la zona (se sono coinvolte solo alcune sottoclassi l'aumento può essere più anodico o catodico),
nel caso delle IgA, un aumento in zona Beta-Gamma formmando il cosidetto «ponte»,
nel caso delle IgM, un addensamento sul punto di semina.
ZONA GAMMA
· L'aumento policlonale delle Ig, anche se molto aspecifico, può però essere utile nella valutazione del decorso clinico di alcune condizioni morbose (lupus, artrite reumatoide, epatite acuta virale).
· Nelle malattie epatiche croniche l'ispezione del tracciato può essere utile nella diagnostica differenziale in quanto si ha aumento di IgA nella cirrosi alcoolica, di lgM nella cirrosi biliare primitiva, di IgG nell'epatite cronica attiva.
ZONA GAMMA
· L'elettroforesi delle sieroproteine e' l'unico metodo analitico a nostra disposizione capace di evidenziare quelle alterazioni qualitative rappresentate dalle GAMMAPATIE MONOCLONALI (MGUS).
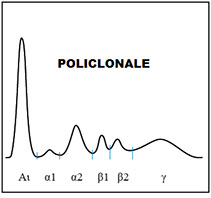
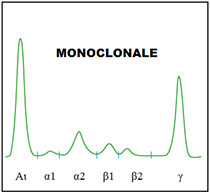
ZONA GAMMA
· Diminuzione: ipogammaglobulinemie congenite e acquisite.
· Aumento policlonale: fisiologico nella risposta anticorpale agli agenti patogeni, patologico nelle malattie croniche con disordine immunitario quali epatopatie croniche, malattie dei collagane e disordini autoimmunitari.
· Aumento monoclonale: gammapatie monoclonali.
Tecniche di Routine
Le tecniche di routine disponibili in laboratorio consentono di accertare alcune delle possibili varianti o anomalie delle proteine (PT)
· Lo studio delle PT ha bisogno di tre elementi fondamentali:
· Qualità
· Concentrazione
· Funzione
Qualità
· Ha due caratteristiche discriminanti.
1. Individualità antigenica o composizione
2. Mobilità elettroforetica o distribuzione
Una tecnica separativa come l’EF(elettroforesi) evidenzia se le frazioni del campione in esame sono simili per distribuzione ad un campione normale, ma non è in grado di evidenziarne la composizione proteica.
Una tecnica immunologica come un dosaggio nefelometrico evidenzia se una proteina è presente nel campione e la sua concentrazione, ma non è in grado di prevederne la distribuzione in una tecnica separativa.
Concentrazione
Con una tecnica separativa possiamo valutare la concentrazione delle proteine totali presenti nelle singole frazioni.
Con una tecnica immunologica possiamo dosare la concentrazione nel campione della singola proteina, cioè della individualità antigenica.
Per valutare la concentrazione delle singole PT presenti in una frazione si dovrà prevedere l’uso di entrambe le tecniche.
Metodi
Per il DOSAGGIO IN FASE LIQUIDA si possono usare la nefelometria o la turbidimetria.
NEFELOMETRIA: l’antigene reagisce con un anticorpo dotato di alta specificità contro quella specifica proteina
Complesso antigene-anticorpo specifico, anche in presenza di altre proteine.
Il fascio di luce del nefelometro viene deviato (scatter) è la deviazione è tanto maggiore quanto più numerosi e più grandi sono i complessi e quindi la concentrazione della proteina
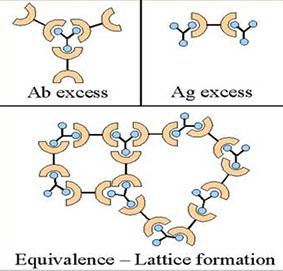
TURBIDIMETRIA: è una tecnica in assorbimento che utilizza un normale spettrofotometro. Esiste una relazione lineare fra assorbanza e concentrazione
>